塞力斯新闻动态
为客户提供最新医疗资讯和优质服务
LeviCell™ 应用场景 | 磁悬浮分选技术助力大火的MSC细胞治疗
2023/03/30


LeviCell™独创的磁悬浮黑科技,能够无需抗体和染色就进行高效的活细胞富集,最大程度的保存细胞活性、原始表型,减少分选过程带来的细胞损失。今天我们就在冻存样本中分别用LeviCell™和常用的流式分选方法来富集复苏的活细胞,再通过下游的单细胞转录组测序(scRNA-seq)结果来对比两种样本处理流程的优劣。
【样本】:
冻存的人多发性骨髓瘤活检样本
【样本处理方式】:
1)不富集
2)流式分选富集活细胞
3)LeviCell™富集活细胞
【结果对比标准】:
scRNA-seq结果数据中,单个细胞中线粒体DNA的百分比上限不得超过10%(严格标准stringent value)或者20%(宽松lenient value)
【结果对比参数】:
在严格或者宽松标准下,去除的低质量细胞数量占比
【结果判读】:
在同一标准下,去除细胞占比越低,说明该样本处理流程保留了更多有效的细胞数据,结果更优
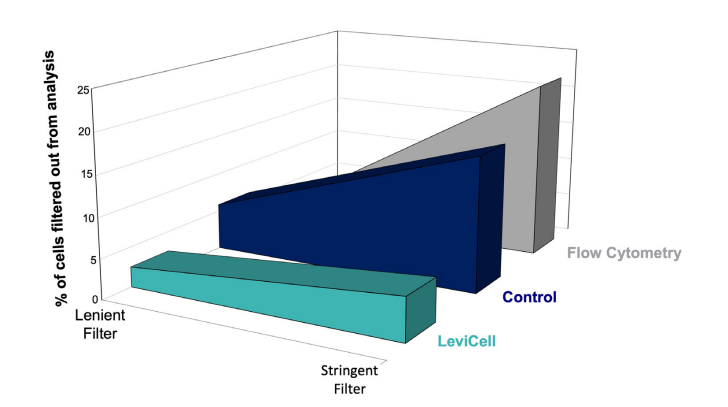
图一:从所有三个工作流的分析中剔除出的细胞占比。左边是宽松标准,右边是严格标准下的结果。
如图一结果所示,在最严格的过滤标准(10%)下,流式细胞术和不富集的样本处理流程导致的细胞数据集剔除比LeviCell™流程分别多4倍和3倍以上。这一结果强调了在scRNA-seq样本处理环节中引入LeviCell™活细胞富集工作流程的价值。

截至2020年8月7日,根据ClinicalTrial.gov网站统计的MSC细胞治疗进入临床实验阶段的项目就有4,044个,仅次于Car-T的相关项目数量,可见,MSC细胞治疗的火爆程度。尽管MSC已经在临床实验中应用于各种疾病的治疗,但是令人惊讶的是我们对MSC作用的机制了解知之甚少。
MSC治疗研究的最大难题在于该类细胞的异质性。MSC可以从各种组织中分离出来,如骨髓、脐带、胎盘和脂肪组织,这引入了组织依赖性的变异,也可能因供体而产生治疗效果的差异。因此,我们需要对MSC来源组织和供体的异质性进行研究,并确定潜在的表型特征Marker,这些Marker最终可以用作MSC细胞治疗产品的疗效预测标志物或关键质量指标,并了解其临床作用机制。我们今天介绍的这篇研究就是用单细胞转录组测序scRNA-seq来比较不同组织、供体来源的MSC细胞的基因表达异质性。
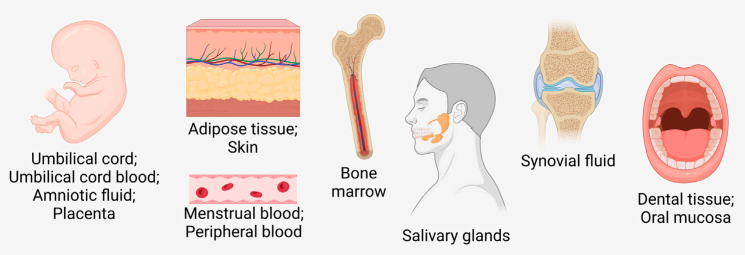
图二:不同组织来源的MSC细胞

Medrano-Trochez(2021年)等比较了最主要的两个来源组织(即骨髓和脐带)中MSC细胞的scRNA-seq测序数据,对比了它们的基因聚类分析(Gene Ontology)结果。结果如图三所示,骨髓来源的间充质干细胞BM-MSC中脂质和脂蛋白代谢、胆固醇生物合成、线粒体转运和代谢途径富集,而脐带来源的间充质干细胞UCT-MSC中ECM组织、胶原生物合成和信号转导富集。这也预示了两种来源的MSC细胞产品潜在的治疗作用存在不同。
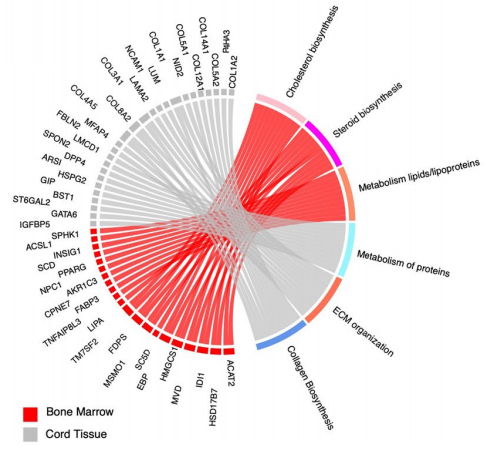
图三:scRNA-seq检测的两种来源的间充质干细胞的基因表达聚类分析。红色聚类基因为骨髓来源的MSC细胞,灰色聚类基因为脐带来源的MSC细胞。
另外,该研究作者还比较了冻存-复苏前后的BM-MSC细胞的基因表达情况变化。结果显示,在冷冻前样本中过表达的一些途径是细胞因子信号传导、细胞增殖和细胞粘附相关基因,而冷冻后则是碳水化合物的相互转化,胆固醇/类固醇生物合成和调节细胞凋亡相关的。其实,除了组织来源和样本冻存带来的MSC细胞异质性,不同的MSC样本供体也会引起细胞基因表达的差异,进一步造成MSC细胞产品的差异和治疗效果的不确定性。
通过进一步的差异基因的PCA主成因分析,作者发现细胞周期相关基因的表达差异是引起MSC产品异质性的主要因素。因此,既可以通过这些基因Marker来判断和预测MSC产品的效果,也可以用来作为相关细胞治疗产品生产的一个质量控制标准。
参考文献
Medrano-Trochez et al. Stem Cell Res Ther (2021) 12:565




新闻推荐
2023.02.24
新机遇 | 国家级创新中心赋能塞力医检创新项目转化
2023.02.16
解密肠道微生态 看塞力医疗如何抢跑健康新赛道?